Geheimnisvolle Alltagsmaterialien
Metalle sind alltäglich. Sie begegnen uns überall. Wir glauben Sie zu kennen, wissen aber eigentlich nichts über sie. Ohne Metalle gäbe es unsere heutige Welt nicht. Sie sind ein unverzichtbarer Bestandteil unserer Technik, haben gemeinsame aber auch unterschiedliche Eigenschaften. Wir glauben, ein Metall zu erkennen, wenn wir es sehen. Wir können aber nicht sagen, was es eigentlich ausmacht, dass ein Stoff ein Metall ist. Zeit, das Geheimnis der Metalle zu lüften!
Fragt man jemanden, was ein Metall ist, wird der meist nicht lange nachdenken: „Eisen ist ein Metall. Kupfer auch. Und natürlich auch Gold und Silber. Und…“ Auch von gelernten Metallern bekommt man in aller Regel eine derartige Antwort. Ein Metaller – und auch viele andere Menschen – kennt ein Metall, wenn er eines sieht. Das denkt er zumindest.

Die obige Antwort auf die Frage, was denn ein Metall sei, ist ja lediglich eine Aufzählung von Metallen. Keine falsche Antwort, aber sie sagt uns nicht, woran man es festmacht, ob ein Stoff ein Metall ist oder nicht.
Etwas näheren Aufschluss geben da schon die Eigenschaften, die wir mit Metallen in Verbindung bringen: Metalle sind typischerweise elastisch, aber auch plastisch verformbar. Sie leiten elektrischen Strom und Wärme. Und wenn man sie glatt genug macht, glänzen sie auf eine ganz bestimmte Art und Weise. Daran erkennen wir ein Metall, wenn wir eines sehen. Aber es wirft auch die Frage auf, warum Metalle diese typischen Metalleigenschaften haben?
Metall in unserer Welt
Schon vor vielen Jahren las ich in einem sehr guten Buch über Metall eine einführende Geschichte, welche die Bedeutung der Metalle für unser Leben drastisch darstellte: Ein Hochofenarbeiter beschickte sich in seiner Stammkneipe. Während einer besoffenen Debatte geriet er in Wut über seinen Beruf, das Eisen und alle Metalle überhaupt. Daheim in seinem Zimmer räsonierte er weiter vor sich hin. Schließlich wünschte er alle Metalle zum Teufel. Auf einmal war da eine gespenstische Gestalt, die ihm diesen Wunsch erfüllte, und ihn durch eine Welt ohne Metalle führte.
Natürlich waren der Hochofen, an dem der Mann arbeitete, ja das ganze Hüttenwerk in sich zusammen gefallen. Alles was aus Metall war, war verschwunden. In der Stadt waren die Häuser zusammengebrochen, weil schlagartig alles Metall daraus verschwunden war. Die geheimnisvolle Gestalt erklärte dem Hochofenarbeiter, das durch seinen Wunsch natürlich alle Gegenstände verschwunden waren, die aus Metallen als Werkstoff gefertigt waren. Und nun sollte der Hochofenarbeiter seine Welt ohne Metalle aufbauen.

Der Hochofenarbeiter schlug Techniken vor, die ohne Metall auskamen. Den Zahn zog ihm aber der Unbekannte und erklärte ihm, dass schließlich alles Metall weg war. Also das auch alle die Werkstoffe fehlten, die wie viele Mineralien, chemische Verbindungen von Metallen darstellen. Mit Keramik und dergleichen war es also auch nichts.
Schließlich erfuhr der Hochofenarbeiter auch noch, dass er sich den Aufbau einer Welt ohne Metall sowieso sparen könne: Auch in allen Lebewesen, sind Metalle enthalten und ohne diese können Sie auf die Dauer nicht leben. Es würde also bald gar keine Menschen mehr geben, die in einer Welt ohne Metall leben könnten.
Mittlerweile hatten die Leute mitbekommen, wer an dem ganzen Chaos schuld war. Sie wollten den Hüttenarbeiter lynchen. Zum Glück wachte dieser jetzt auf, denn er hatte den ganzen Schlamassel nur geträumt. Und heilfroh darüber, dass es alle Metalle doch noch gab, trat er seinen morgendlichen Arbeitsweg an.
Wo überall Metall drin steckt
Tatsächlich wäre eine Welt ohne Metall nicht möglich. Die Geschichte von der Welt ohne Metall hat übrigens einen kleinen Fehler: Wenn wirklich alle Metalle aus der Welt verschwunden wären, hätte der Hochofenarbeiter keine Chance mehr gehabt, sich diese Welt ohne Metall anzusehen. Der Autor hat nämlich eines übersehen: Es wird zwar gesagt, dass die winzigen Mengen an Metallen in unserem Körper, die wir Spurenelemente nennen, lebenswichtig sind. Aber nicht, dass wir eine deutlich größere Menge an einem Metall im Körper haben, ohne das wir in kürzester Zeit tot wären.
Die Menge an Eisen, welche wir im Körper haben, ist nämlich sehr viel größer, als die Mengen an sonstigen Metallen. Das Eisen ist ein wichtiger Bestandteil unseres roten Blutfarbstoffs und damit unverzichtbar für den Sauerstofftransport. Nach dem Verschwinden aller Metalle wäre der Hochofenarbeiter aus unserer Geschichte und natürlich alle anderen Leute auch in kürzester Zeit erstickt.

Metalle finden sich also in allen möglichen Stoffen, die äußerlich gar nicht nach Metall aussehen. Das sind zum Beispiel Mineralien wie Kalkstein, der das Metall Kalzium enthält. Im Salz, dass wir uns aus Frühstücksei streuen, steckt außer Chlor auch Natrium. Letzteres ist ebenfalls ein Metall. Eisen steckt außer im Blut und im Fleisch auch in Pflanzen. Mit dem vermeintlich hohen Eisengehalt des Spinats hatte man sich zwar vertan, aber er enthält Eisen. Auch Zink steckt im Fleisch und ist für unseren Hormonhaushalt wichtig. Wenn uns Magnesium fehlt, plagen uns Muskelkrämpfe. Dagegen helfen Bananen, welche allerhand davon enthalten.
Chemische Elemente und Atome
Die Liste der Dinge, die Metalle enthalten, könnte man noch lange fortsetzen. Sie erklären uns aber immer noch nicht, was das eigentliche Wesen eines Metalls ist. Metalle sind chemische Elemente, die eine ganz bestimmte Struktur bilden. Chemische Elemente sind Stoffe, die nur aus einer einzigen Art Atome bestehen und damit die Grundbausteine der Chemie.
Ein Atom besteht aus einem Atomkern und einer Hülle. Der Atomkern wird von Protonen gebildet, die eine Masse besitzen und elektrisch positiv geladen. Bei vielen chemischen Elementen sitzen im Kern auch noch Neutronen, die elektrisch neutral sind. Ein Neutron hat aber die gleiche Masse wie ein Proton. Die Hülle des Atoms besteht aus Elektronen, die elektrisch negativ geladen sind und so gut wie keine Masse haben.
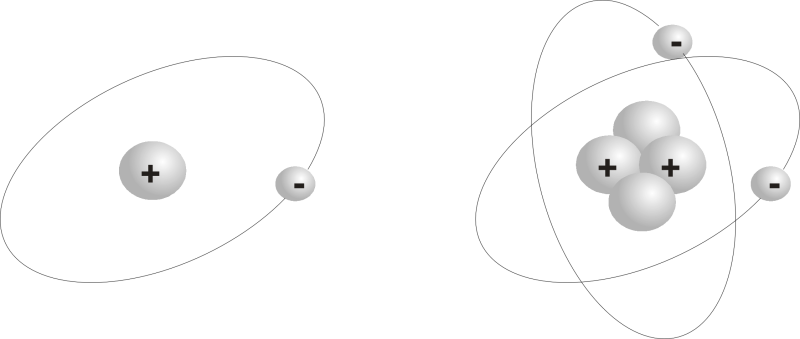
Damit das Atom nach außen elektrisch neutral ist, muss es immer genau so viel Elektronen geben wie Protonen. Die Zahl der Neutronen hat lediglich Einfluss darauf, wie schwer das chemische Element ist, nicht jedoch auf seine chemischen Eigenschaften. Die wird allein durch die Anzahl der Protonen und Elektronen bestimmt. Die Anzahl der Neutronen kann beim gleichen chemischen Element variieren. Die Varianten mit unterschiedlichen Neutronenzahlen nennt man dann die Isotope dieses Elements. Entscheidend aber ist immer die Anzahl der Protonen im Kern und der zugehörigen Elektronen.
Baukastensystem Atom
Mit den Protonen und den Elektronen hat man so eine Art Baukastensystem für Atome: Man nimmt ein Proton oder mehrere für den Kern und die entsprechende Anzahl von Elektronen für die Hülle. Ein einziges Proton und das zugehörige Elektron bilden das einfachste Atom überhaupt. Das ist der Wasserstoff den wir links im obigen Bild sehen. Daneben sehen wir das nächst größere Atom, das Helium mit zwei Protonen und zwei Elektronen. Hier gibt es noch zwei Neutronen, die aber lediglich das Atom schwerer machen. Seine chemischen Eigenschaften kommen von den zwei Elektronen, die es haben muss, weil es zwei Protonen hat.
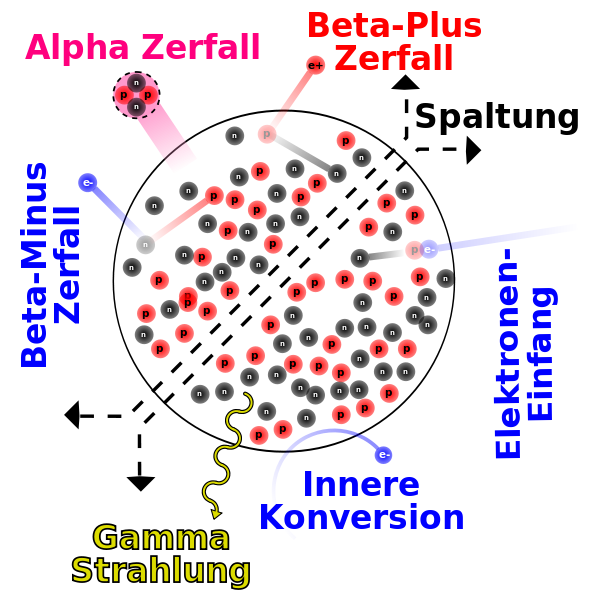
Dieses Baukastensystem kann man nun fortsetzen bis zu Atomen mit ungefähr 100 Protonen. Wenn aber zu viele Protonen in einem Atomkern sitzen, ist das so, wie wenn man sich zu viele Eiskugeln auf die Waffeltüte packen lässt: Die Geschichte wird instabil. Die richtig großen Atomkerne neigen daher dazu, zu zerfallen. Das nennt man Radioaktivität. Die chemischen Elemente mit den vielen Protonen bestehen daher nicht lange.
Das spielt für unsere Geschichte aber keine Rolle. Wichtig ist, dass die Anzahl der Protonen und damit der Elektronen in einem Atom bestimmt, um welches chemische Element es sich handelt. Was uns im Hinblick auf die Metalle dabei besonders interessiert sind die Elektronen.
Metalle sind Kristalle
Jeder hat schon einen Kristall gesehen. Viele chemische Elemente und Verbindungen bilden Kristalle. Kochsalz zum Beispiel, aber auch Zucker und sogar Wasser – wenn es gefriert. Quarz, den wir als Bergkristall kennen und eine ganze Menge andere Mineralien.
Metalle sind Kristalle – das reimt sich und was sich reimt ist gut, würde der Pumuckl sagen. Und wäre wahrscheinlich zufrieden. Uns kommt das aber komisch vor: Da liegt ein 6 m langes 200er U-Eisen und das soll ein Kristall sein? Jein, muss die unklare Antwort lauten.
Man muss hier etwas genauer hinsehen. In der Tat ist ein Stück Metall wie ein U-Eisen oder 20 cm Kupferdraht kein monolithischer Kristall, also ein Kristall aus einem Stück. Wenn man Metall nun aber anschleift und anätzt, offenbart es unter dem Mikroskop seine Struktur. Was man sieht, sind kleine Körnchen. Sie können verschieden groß sein, aber sie sind immer da. Und jedes dieser Körnchen ist ein kleiner Kristall.
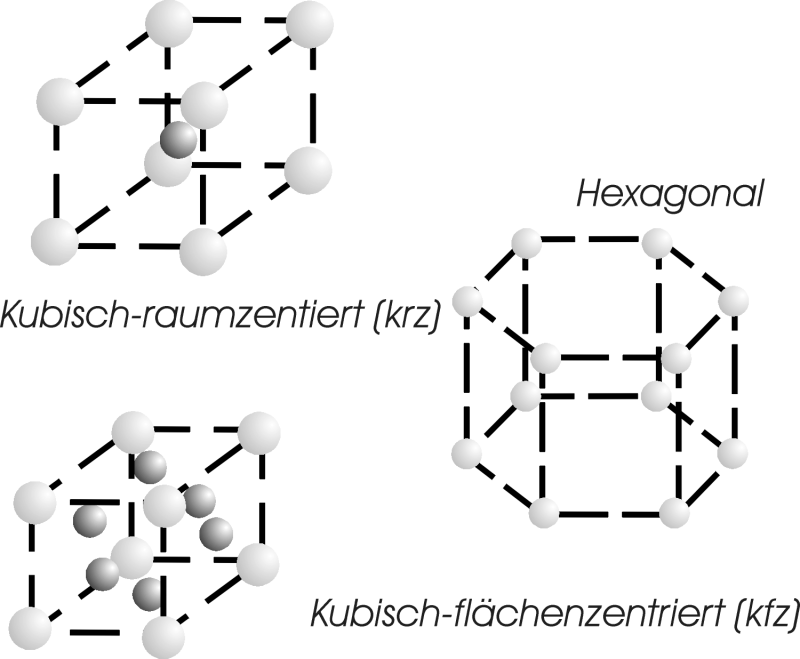
Ein Kristall ist ein Stück Material, bei dem die Atome oder Moleküle in einer jeweils ganz bestimmten Art als räumliches Gitter angeordnet sind. Das passiert, wenn da bestimmte Kräfte wirken. Manche Stoffe tun das, andere nicht. Bei denen, die das nicht tun liegen die Atome oder Moleküle irgendwie beieinander, ohne dass es da eine bestimmte Regel. Einen solchen Stoff nennt man amorph. Manche Stoffe können sowohl kristallin als auch amorph daherkommen. Der Kohlenstoff zum Beispiel kann amorph sein – das ist dann Ruß – aber auch zwei verschiedene Kristalle bilden: den Graphit und den Diamanten.
Kristalle mit Besonderheit
Im Bild unten sieht man das Kristallgefüge eines Metalls. Es ist ein sogenanntes kubisches Gitter, weil die Atome ein rechtwinkliges räumliches Gitter bilden und die Abstände nach oben und unten, nach links oder rechts sowie vorne und hinten gleich sind. Auf gut Deutsch gesagt: Es besteht aus lauter kleinen Würfeln. Das könnte beispielsweise Eisen sein, denn Eisen hat einen kubischen Kristall. Es gibt aber auch andere Metalle mit dieser Struktur. Beim Kupfer sind es hingegen sechseckige Säulen, aber das spielt in diesem Zusammenhang keine Rolle.
Das Entscheidende ist die Besonderheit dieses Kristalls. Die Atome, die ihn bilden sind elektrisch geladen. Elektrisch geladen ist ein Atom, wenn ihm Elektronen fehlen oder es zu viel Elektronen hat. Man spricht dann von einem Ion. Fehlen ein oder mehrere Elektronen, überwiegt die positive Ladung der Protonen im Kern. Dann hat man ein positives Ion. Gibt es ein oder mehrere Elektronen zu viel, hat man ein negatives Ion.
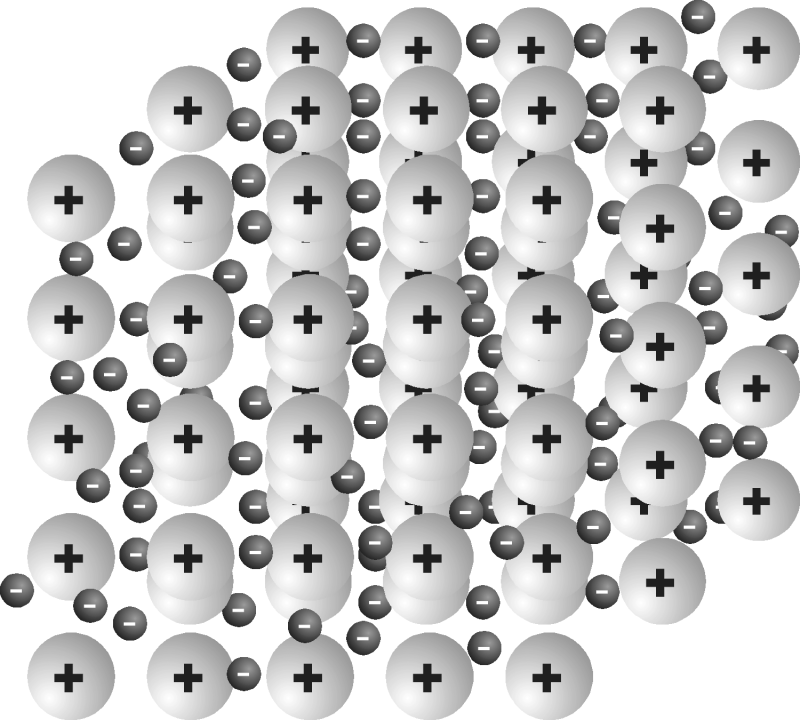
Bei der Kristallstruktur von Metallen ist nun etwas passiert, dass bei anderen Kristallen nicht passiert: Im Durchschnitt ein Elektron pro Atom hat sich unerlaubt von der Truppe entfernt. Es ist nicht mehr da, wo es eigentlich hingehört, sondern treibt sich lustig umher zwischen den Metallionen, die das Gitter bilden.
Diese Elektronen, die sich im Gitter umher treiben bezeichnet man als freie Elektronen. Man sagt auch Elektronengas, weil sie gegeneinander frei beweglich sind, wie die Atome oder Moleküle eines Gases. Und diese freien Elektronen oder das Elektronengas sind nun das, was einen Stoff als Metall definiert.
Das Elektronengas und die typische Verformbarkeit von Metall
Die freien Elektronen in einem Metall sind ja elektrisch negativ. Die Metallatome oder besser -ionen, die das Gitter bilden sind positiv. Deswegen ziehen sich Metallionen und Elektronengas gegenseitig an. Zwischen den Metallionen bestehen natürlich auch die Kristallkräfte, die jeden Kristall zusammenhalten und in seine Form bringen. Hier gibt es aber mit dem Elektronengas so eine Art elastischen Kleister, der das ganze zusätzlich stabilisiert.

Stellen wir uns vor, die Struktur im Bild ist ein winziger Ausschnitt aus einem Kristall in einem Flacheisen, dass jemand in einen Schraubstock eingespannt. Wenn dieser Jemand nun gegen dieses Flacheisen drückt, gibt es etwas nach. Dabei verschieben sich die Kristallionen ein wenig gegeneinander. Das Elektronengas hält nun mit seiner Kleisterwirkung dagegen. Lässt der Bursche das Eisen los, geht es in seine Ausgangslage zurück, weil der Elektronengas-Kleister es zurückzieht. Das ist die elastische Verformung.
Nun drückt der Kerl stärker gegen das Eisen. Irgendwann wird das dem Elektronengas-Kleister zu viel und er reißt ab. Jetzt verschieben sich die Kristallionen gegeneinander – das Flacheisen verbiegt sich. Wer schon mal ein Stück Stahl gebogen hat, weiß, dass es an einem bestimmten Punkt auf einmal leichter geht und so eine Art Ruck gibt. Das ist der Moment, wenn das Elektronengas loslässt.
In der neuen Position aber kleistert das Elektronengas den Kristall sofort wieder zusammen und zieht ihn dabei auch noch ein Stückchen zurück. Dadurch ist das gebogene Flacheisen auch wieder stabil, nachdem es ein kleines Stückchen zurückgefedert hat. Jeder, der mit Metall arbeitet, weiß, dass man immer ein Stückchen über den Winkel hinausbiegen muss, den man haben will. So stimmt der Winkel dann nach dem Zurückfedern.
So haben wir schon mal zwei der typischen Metalleigenschaften aus dem typischen Aufbau der Metalle erklärt: die plastische und die elastische Verformbarkeit.

Wärmeleitfähigkeit und elektrische Leitfähigkeit
Stellen wir uns nun vor, man macht einen Rundstahl warm, indem man ihn in ein Schmiedefeuer hält. Wenn das kein langer Rundstahl ist, gibt das ganz schnell Aua an der Hand. Das Metall hat die Wärme des Schmiedefeuers fix bis zu unserer Hand geleitet.
Wärme in Körpern ist nun nichts anderes als Schwingung der Teilchen. Je wärmer ein Stoff ist, umso schneller schwingen seine Atome bzw. Moleküle. Deswegen gibt es bei der Temperatur auch diesen absoluten Nullpunkt: Bei diesen 0 K oder -273 °C gibt es keine Teilchenschwingungen mehr und weniger als nichts gibt es nicht.
Wärmeleitung ist nun nichts anderes, als die Fortpflanzung dieser Teilchenschwingungen durch einen Körper. Je je leichter sich die Schwingung überträgt, umso besser die Wärmeleitfähigkeit. Bei den Metallen hilft das Elektronengas mächtig mit, diese Schwingungen zu übertragen und deswegen sind Metalle gute Wärmeleiter.

Halten wir nun einen elektrischen Pluspol an ein Stück Metall. Ein elektrischer Pluspol ist ein Ort mit Elektronenmangel. Weil dort mehr Platz vorhanden ist, werden die freien Elektronen aus dem Metall in den elektrischen Pluspol drängeln. Verbindet man nun das andere Ende mit einem elektrischen Minuspol – das ist ein Ort mit Elektronenüberschuss – marschieren die freien Elektronen aus unserem Stück Metall in den Pluspol und aus dem Minuspol kommen ständig Elektronen nach. Durch das Metall fließt ein elektrischer Strom.
Außer der Wärmeleitfähigkeit kommt also auch die elektrische Leitfähigkeit der Metalle von ihrem inneren Aufbau mit dem Elektronengas. Elektrische Leitungen in Festkörpern findet übrigens ausschließlich auf diese Art statt. Sie ist nur möglich, wenn es freie Elektronen gibt. Und die gibt es nur bei Metallen und bei allen Metallen. Daher sind alle Metalle mehr oder weniger gute elektrische Leiter und alles Feste, was den elektrischen Strom leitet ein Metall.
Schließlich kommt auch noch der typische Metallglanz von diesem inneren Aufbau der Metalle. An einer glatten Oberfläche bewirkt das Elektronengas, dass das Licht auf dieses besondere Art reflektiert wird, die wir als Metallglanz kennen.
Ist der Kohlenstoff etwa ein Metall?
Keine Regel ohne Ausnahme heißt es nun. Der Kohlenstoff gilt bekanntlich als Nichtmetall. Seine amorphe Form, der Ruß, leitet den elektrischen Strom nicht. Auch die eine kristalline Form, der Diamant, ist ein Isolator. Aber der andere Kristall, der Graphit, der leitet den elektrischen Strom. Zwar nicht besonders gut, denn er hat nur wenige freie Elektronen. Aber er tut es, weil er eben ein paar solche freie Elektronen hat.
Na sowas! Da gibt es doch tatsächlich ein Nichtmetall, das den elektrischen Strom leitet! Naja, sagt da so mancher Chemiker, das ist doch kein Problem. Wenn sich der Kohlenstoff in seiner Erscheinungsform Graphit so verhält, soll er doch als Graphit ein Metall sein. Und in den beiden anderen Erscheinungsformen ist er eben ein Nichtmetall. Tatsächlich kann man es so sehen und damit den Widerspruch auflösen.
Und übrigens ist der Kohlenstoff ein ganz besonderer Stoff, der für unsere Welt eine große Role spielt. Ohne ihn gäbe es weder unsere Natur noch unsere Technik. Aber das ist Stoff für eine andere Geschichte…
4 Pingbacks